Annonse
Charcot fot
Charcot fot er en alvorlig inflammasjon (betennelse) av foten som ubehandlet fører til grove deformiteter av foten. Tilstanden sees oftest hos pasienter med diabetes og samtidig nevropati men kan også oppstå hos ellers friske mennesker. De patofyisologiske mekanismene bak denne tilstanden er ikke helt kjent, men en vet at en dysregulering av de autonome nervene er involvert. I mange tilfeller ser en at det oppstår i etterkant av små traumer eller skader av foten, men tilstanden kan også oppstå spontant.
Charcot fot kalles også Charcot artropati eller nevroartropati. Tilstanden ble først beskrevet av den franske nevrologen Jean Martin Charcot i 1868. I den tiden var syfilis en vanlig årsak for utvikling av Charcot artropati. I dag er det som nevnt ovenfor i hovedsak pasienter med diabetes som rammes av denne tilstanden. Charcot fot kan også oppstå hos pasienter som får nevropati av andre sykdommer som HIV/AIDS, arvelig nevropati, alkoholisme, meningomyelocele (ryggmargsbrokk) tverrsnittlesjoner, ved revmatisme, pasienter som har gjennomgått pancreas- eller nyre transplantasjon og hos dialyse pasienter. Også pasienter som nylig har fått utført revaskularisering (for eksempel utblokking/stenting av leggarterier) er mer utsatt for å bli rammet av denne tilstanden. Overvekt ansees også som en risikofaktor.

Figur 1 Jean Martin Charcot (1825-1893) var en anerkjent fransk nevrolog som forsket på alt mulig innen nevrologi. Han er kjent som grunnleggeren av den moderne nevrologien og hans navn er assosiert med minst 15 medisinske eponymer, blant annet Charcot-Marie-Tooth sykdom og Charcot artropati. Om en skal være helt korrekt så var det først i 1936 at den amerikanske legen William Riely Jordan beskrev den klare sammenheng mellom diabetes nevropati og fare for utviklingen av Charcot fot. Copyright: Wikipedia
Charcot artropati kan i prinsippet ramme hvilket som helst vektbærende ledd i kroppen men en ser det nesten alltid i underekstremitetene, spesielt i ankel og fot. Oftest rammes bare en side av kroppen men hos 10% oppstår Charcot i begge underekstremitetene samtidig. Noen studier tyder på at menn og kvinner rammes omtrent likt av dette, andre studier tyder på at menn er tre ganger mer rammet av Charcot fot. Når tilstanden først er «utbrent» er det sjelden at den dukker opp igjen, sannsynligvis får mindre enn 5% tilstanden på nytt.
Dessverre er det fortsatt overraskende mange sårbehandlere som aldri har hørt om tilstanden, selv om opptil 2,5% av pasienter med diabetes vil utvikle Charcot fot i løpet av livet sitt. Dette fører til vesentlige forsinkelser i behandlingen. I en artikkel fra Podiatry Today var den gjennomsnittlige forsinkelsen før diagnosen var stilt 29 uker! Dette gjaldt USA, men det er ingen grunn til å anta at forholdene er vesentlig bedre i Norge.
Kliniske Funn
Den typiske pasienten som utvikler Charcot fot er som regel i femti årene, har hatt diabetes i over 10 år eller en dårlig regulert diabetes. Pasienten er ofte overvektig.
Det kliniske bildet kan variere mye noe som ofte fører til forsinkelsen av diagnosen. Felles for de fleste er hevelse og varme i foten. Merk imidlertid at hevelse og varmeutvikling kan være diskre hos noen men uttalt hos andre. En temperaturforskjell av mer enn 2 C° er suspekt, hos noen kan temperaturen være opptil 7 grader høyere i den affiserte foten. Ofte ser en også erythem (rødme) i huden, den kan være så uttalt at en først tenker på infeksjon.

Figur 2 Det klassiske kliniske bilde av akutt Charcot fot er en hoven, rødlig og varm fot. Klinisk ligner tilstanden veldig på infeksjon og blir som regel feiltolket slik. Mange av pasienter blir derfor feilaktig satt på antibiotika. Først når en ser at antibiotikaen ikke fører til bedring kommer noen på tanken at det kan være noe annet enn infeksjon. Husk at Charcot artropati kan ramme hvilken som helst ledd i kroppen men oftest er det underekstremiteten, oftest ensidig.

Figur 3 Denne pasienten klaget over hevelse, rødme og varme i foten i over et halvt år før hun ble henvist til en spesialpoliklinikk. Hun har ikke kjent diabetes og ingen andre kjente risikofaktorer. Temperaturmålingen viser over 3 graders forskjell mellom den friske høyre og den affiserte venstre foten. Legg merke til at den rammete foten ikke er så påfallende hoven og rød, i noen tilfeller kan tilstanden være mer mild/moderat. Merk at temperaturen en måler er overflatetemperaturen. Den er alltid noen grader lavere enn kroppstemperatur.
Selv om vi oftest kan kjenne temperaturforskjell med hendene våre er det nyttig å ha tilgang til et infrarødt termometer for å dokumentere temperaturen. Også senere i forløpet mens pasienten er under behandling vil det være nyttig å kunne dokumentere at temperaturen gradvis går nedover. Alle termometre som ikke må holdes rett på huden bruker infrarødt (IR) prinsipp. Vi har testet to febertermometre kjøpt på apotek til dette formålet, men fikk veldig varierende resultater når vi målte på føtter. Det IR termometeret som fungerte best i våre hender er modellen vist i fig 4 nedenfor, det leverte stabile og reproduserbare målinger. Termometeret er kjøpt hos Biltema.

Figur 4 Dette infrarøde termometeret fra Biltema koster cirka 550.- NOK, vi fant at det var bedre egnet til å måle temperaturen under føttene enn noen av de vanlige febertermometrene som også fungerer på infrarød basis.
Selv om mange av pasienter med Charcot fot har sensorisk nevropati, rapporter likevel cirka 75% av pasientene noen grad av smerter. Om en ikke vet om pasienten har nevropati er det obligatorisk å undersøke dette med en 10g -monofilament test (se også vårt kapittel om monofilament undersøkelse)
Cirka 40% av diabetes pasientene med Charcot fot har et fotsår samtidig, dette fører ofte til at den varme foten blir feildiagnostisert og at en mistenker infeksjon. Pasienten får ordinert antibiotika som han/hun ikke trenger.
Når knoklene begynner å bli rammet kan en av og til kjenne at leddene virker løse ved undersøkelse. Ved langkommet Charcot fot ser en deformiteter i foten, veldig typisk ser en kollaps av midtfot (nedsunken midtfot) som en kaller vuggemeiefot når det er uttalt.
Videre Utredning
Det er viktig at fastlegen henviser pasienten til en ortopedisk avdeling med en gang en har mistanke om denne tilstanden. Videre utredning og behandling skal foregå i spesialisthelsetjenesten, helst tverrfaglig.
Blodprøver
Det finnes ingen blodprøve som kan bekrefte eller avkrefte Charcot fot, men vi må benytte oss av blodprøver for å utelukke andre tilstander. En viktig differensialdiagnose er infeksjon (cellulitt, erysipel, abscess og osteomyelitt) og i utredningen hører det derfor med at vi tar blodprøver for å sjekke for en bakteriell infeksjon: LPK (hvite blodlegemer), CRP, prokalsitonin og senkning. Ved en Charcot fot vil noen disse prøvene også være forhøyet men mer moderat enn ved en infeksjon. Blodprøven prokalsitonin kan av og til være nyttig til å differensiere mellom bakteriell infeksjon og inflammasjon.
En annen viktig differensialdiagnose er urinsyregikt, det må derfor bestilles S- urat prøve.
I tillegg skal man sjekke blodsukker, HbA1c, nyreverdier og vit B12. Hvis Charcot fot oppstår plutselig hos friske personer bør en utrede videre med alkalisk fosfatase, kalsium, fosfor og paratyroidea hormon for å sjekke for skjelett sykdommer som Pagets sykdom. Hyperkalsemi kan tyde på kreft eller metastaser i knoklene. En anamnese om alkoholbruk hører også med i utredningen og måling av fosfatidyletanol kan avdekke en evtl skult alkoholmisbruk som årsak til utvikling av Charcot fot.
Selv om syfilis er blitt sjelden i Norge så må en ha den diagnosen i bakhodet som en mulig forklaring for en spontan oppstått Charcot fot hos en ellers frisk person. Syfilis diagnosen stilles med immunologiske blodprøver, av og til spinal punksjon.
Radiologisk utredning
Videre utredning med radiologiske modaliteter er obligatorisk for å bestemme alvorlighetsgraden av tilstanden, og for å utelukke andre årsaker som for eksempel infeksjon/osteomyelitt.
Oftest begynner en utredningen med vanlige røntgenbilder selv om en stort sett alltid supplerer med magnet resonans (MR) undersøkelse. Grunnen til dette er at en helst vil ta undersøkelsene under vektbelastning da dette lettere vil avsløre feilstillinger, disse er kanskje ikke er synlig når pasienten ligger på benken. MR bildene kan ikke tas med belastning i Norge. Merk at ikke alle røntgenavdelingene har et godt opplegg for å ta stående bilder med belastning (det er noe teknisk krevende å få røntgen kamera i samme høyde som fotsålen) og det er viktig å spesifisere i henvisningen hvorfor en trenger belastningsbilder. Noen pasienter vil imidlertid ikke klare å stå på en slik innredning pga høy alder, balanseproblemer, andre skader osv. og da må en nøye seg med vanlige røntgenbilder uten belastning. Fig 5 nedenfor viser hvordan pasienten må kunne stå for å ta røntgenbilder med belastning.

Figur 5 Om mulig bør røntgenbildene tas med samtidig belastning. Det er noe teknisk utfordrende for røntgen avdelingen men de fleste avdelinger har et opplegg for dette. Merk også at ikke alle pasienter klarer å stå slik på en fot. Copyright medscape
En supplerer stort sett alltid med MR med kontrast siden det er mer følsom undersøkelse til å påvise forandringer i skjelett og fordi den er mer egnet til å påvise infeksjon/osteomyelitt enn vanlig røntgen.

Figur 6 En MR undersøkelse av venstre fot som viser forandringer i metatars II og III ( røde piler). Når en ser skjelettforandringer i 2 eller flere knokler passer det bedre med Charcot fot enn osteomyelitt. Dette MR bildet er tatt i den tidlige fasen av en Charcot fot tilstand, og dersom en starter med avlastning umiddelbart kan tilstanden fortsatt reverseres helt.
Noen ganger kan det være vanskelig å utelukke en osteomyelitt med MR, i så fall bør en utrede videre med en skjelett scintigrafi. En såkalt leukocytt scintigrafi (indium-111 WBC scan) er ofte brukt da standard technetium scan er noe mindre spesifikk her.
Noen pasienter har også kontraindikasjoner for å ta MR (for eksempel ved visse pacemakere og andre sensitive implantater eller ved allergi for MR kontrastmiddel), da anbefaler en også en leukocytt scintigrafi. Et annet alternativ er en LFDG-PET/CT scan som er en spesiell form for CT som ellers brukes til kreft utredning.
Om pasienten er påfallende hoven i leggen må en også tenke på dyp vene trombose (DVT). Om en ikke kan utelukke en DVT bør en ta en ultralyd av venen i underekstremiteten og blodprøven D-dimer.
Andre undersøkelser
Om pasienten har en uttalt hissig Charcot fot kan blodprøvene CRP og Lpk være relativ høye. Da er det av og til vanskelig å utelukke infeksjon/osteomyelitt også med MR, spesielt om det foreligger et fotsår samtidig. I så fall vil det være behov for en benbiopsi til bakteriell dyrkning.
Som en tommelfinger regel kan en si at dersom pasienten ikke har et fotsår er det mer usannsynlig at vedkommende har en infeksjon/osteomyelitt. Om pasienten derimot har et sår hvor en i tillegg kan sondere ned til ben så må en mistenke osteomyelitt. Senkning er sjelden høyere enn 70 ved Charcot fot, er den > 70 er det oftere tegn på infeksjon.
Om ankelleddet er påfallende hovent og varmt kan det være behov for en leddpunksjon med bakteriell undersøkelse av leddvæsken for å utelukke en septisk artritt. Husk at en selvsagt kan ha en aktiv infeksjon og Charcot fot samtidig. En fotinfeksjon kan føre til utvikling av Charcot fot. Tilstanden er med andre ord ganske komplisert og bør derfor alltid behandles på en avdeling i spesialisthelsetjenesten som har erfaring med Charcot fot.
Klassifikasjon
Det finnes flere klassifikasjonsystemer for Charcot fot. For vår kliniske hverdag er ikke disse så avgjørende, men om en driver med forskning må en kunne forholde seg til disse systemene. Alle har til felles at en klassifiserer alvorlighetsgraden utfra de radiologiske funnene. Her bruker en vanlig røntgen, MR eller CT undersøkelser.
Det enkleste er Brodsky/Rouse klassifikasjonen og for våre behov som sårbehandlere er denne klassifikasjonen oftest tilstrekkelig:
Type 1 involverer forfoten og midtfoten
Type 2 involverer bakfoten
Type 3 involverer ankelen
Mer detaljerte klassifikasjoner er Saunders/Mrdjencovich og Schön klassifikasjonssystemene. Vi går ikke i mer detaljer om disse her, om du ønsker å lese mer om de finnes det rikelig annen online litteratur om disse.
Behandling
Behandling deles inn i den akutte og den post-akutte fasen.
Akutt fasen- Avlastning
I den akutte fasen er avlastning det aller viktigste tiltaket. Her er det ikke tilstrekkelig med ortopediske fotsenger eller gode sko. Det er internasjonal enighet om at den akutte Charcot fot alltid skal behandles med enten en total-contact-gips eller en walker ortose.
Ideell sett skal pasienten ikke belaste foten i det hel tatt i den akutte fasen (total non weight bearing- NWB). Flere studier viser dog at slike strenge restriksjoner fører til dårligere compliance, kanskje i den grad at pasienten ikke vil bruke ortosen i det hele tatt. Her må en altså individualisere rådene. Pasienten må få informasjonen at full vektbelastning i den akutte fasen vil forlenge perioden han/hun må bruke ortosen. Som regel ender det med at en tillater partiell vektbæring, det vil si at pasienten må bruke krykker inntil den akutte fasen er over. Den mest akutte fasen er over når hevelsen avtar og temperaturen i foten synker (krever altså IR termometer for å kunne dokumentere dette).
En god total-contact gips krever en del gipse ferdigheter og veldig få i Norge har erfaring med det. En dårlig anlagt gips kan føre til alvorlige trykkskader som pasienten ikke oppdager i tide fordi han/hun som regel har nevropati. Vi anbefaler derfor at en bruker walker ortoser. Her finnes det mange modeller å velge fra, om en har en ortopediingeniør tilgjengelig er det en stor fordel at walker ortosen tilpasses av ortopediingeniøren, da også en slik ortose kan forårsake uheldig trykk og gnag om den ikke tilpasses korrekt. Dessuten kan det være behov for en spesial såle i walkeren som ortopediingeniør må tilpasse. NB! Pasienten skal få tilpasset støvlene med en gang diagnosen mistenkes, her skal en ikke vente flere dager for å få tak i en slik støvel. Derfor bør alle sårpoliklinikker alltid ha slike på lager i diverse størrelser om en ikke har ortopediingeniør tilstede umiddelbart.
Vi kan ikke si at vi har oversikt over alle modellene og de forskjellige fordelene og ulempene mellom de ulike walkere. På generell basis kan en si at en forventer at walkere med integrerte luftputer som kan blåses opp («air-cast» type walkere) muligens har en fordel fordi de sitter tettere og dermed avlaster enda bedre. På mange arbeidsplasser styres utvalget av walkere gjennom anbud, men husk at pasienten har rett til «hvilken som helst» ortopedisk walker når en søker om dette hos HELFO via skjema «søknad om ortopediske hjelpemidler». For å få litt mer klarhet i denne jungelen av ortopediske walkere skal vi be et ortopedisk firma å komme med en uttalelse her. Når det foreligger legger vi det ut i et nyhetsbrev.

Figur 7 Under tilpasning av en walker ortose. Det er viktig at walkeren passer godt og at den sitter tett mot huden. Det er viktig at pasienten prøver walkeren i cirka 10 min inne hos behandleren slik at han/hun kan teste den godt og sjekke om den passer behagelig.
Oftest kommer det ganske brått på pasienten at han/hun må få en slik stor støvel på foten, den ligner jo nesten på en klumsete skistøvel. Det er vanskelig å gå med og krever god balanse. Noen pasienter vil ha behov for støtte med krykker mens de bruker en slik ortose.
Pasienten må få en nøye forklaring om tilstanden, hvor alvorlig den er og hvorfor det er absolutt indisert med en slik ortose. Pasienten må også informeres om varigheten av behandlingen – han/hun må finne seg i minimum 3 måneders behandling med walker ortosen. Men ikke lov pasienten at det bare blir 3 måneder – da blir pasienten meget skuffet om man må legge til ytterlige 3 måneder fordi tilstanden roet seg langsommere enn forventet. Vi pleier å si til pasienten fra starten at behandlingstiden vel kan strekke seg opptil et halvt år men om hun/han er heldig kan det blir kortere – da har pasienten realistiske forventninger fra starten av.
Det er viktig at pasienten alltid har ortosen på når han/hun belaster foten i behandlingstidsrommet. Selv en liten tur på badet uten ortosen vil kunne føre til en ny oppblussing av tilstanden og forlenge tiden pasienten må ha ortosen. Igjen, dette krever god informasjon til pasienten. Noen pasienter vil kunne følge disse instruksjonene til punkt og prikke mens andre kommer til å variere bruken av ortosen og andre vil ikke bruke støvelen i det hele tatt. Utfordringen med at pasienten som regel ikke kan kjøre bil med ortosen (med mindre at pasienten har automat gir eller el-bil og at det er venstre foten som er rammet) vil gjøre at noen pasienter slurver med bruk av ortosen. Om en har mistanke om at det er dårlig compliance bør en låse ortosen til foten med for eksempel en runde med gips. Noen steder bruker en strips til dette men disse er enklere for pasienten å klippe av med en saks enn en gips. Med andre ord, de pasientene som er mest compliant kan sove om natten uten ortosen på, andre pasienter må bruke ortosen dag og natt og helst ha den låst til foten.

Figur 8 Det finnes et bredt (og noe forvirrende utvalg) av ortopediske walker ortoser som kan brukes for avlastning av Charcot fot. Modellene nederst har integrerte luftputer som kan pumpes opp («air-cast» prinsipp). Det betyr at støvelen oftest vil sitte noe tettere når en bruker en støvel med luftputer. En forventer at støvelen avlaster bedre når den sitter tett mot huden. Etter vår erfaring er det ikke nødvendigvis avgjørende. Det viktigste er at pasienten faktisk bruker den walkeren han/hun har fått og at en sjekker med jevne mellomrom at den fortsatt passer fint.
I USA og noen andre land er total-contact-casting (TCC) altså en tettsittende gips førstevalg i behandlingen, muligens fordi den er rimeligere og på mange sykehus i USA har en også gipsteknikker tilstede som kan være behjelpelige med å lage denne typen spesialgips. Som nevnt ovenfor anbefaler vi walker ortoser til dette i Norge, studier tyder på at resultatene er likeverdig så sant pasienten virkelig bruker sin ortose.
Om en bruker gips så anbefales det at gipsen sjekkes hver uke for å være sikker at den fortsatt passer godt og ikke gnager. Gipsen bør byttes hver uke/hver andre uke avhengig av alvorlighetsgraden av Charcot tilstanden. Pasienter med sår på føttene må kanskje bytte gipsen enda oftere!
Om en bruker en walker ortose må denne også inspiseres regelmessig. Hvor ofte er avhengig av om pasienten har uttalt nevropati, om pasienten har sår samtidig og hvordan den generelle compliance er. Det er alltid fornuftig å ta pasienten inntil en kontroll selv om pasienten ikke har sår bare for å sjekke at alt er i orden. Etter det er det tryggest å avtale kontroller hver andre uke (hyppigere om pasienten har sår). En tett oppfølging vil i tillegg gi en bedre compliance.
Vi anbefaler også bruk av kompresjonsstrømpe under walker ortosen. Vi fant lite dokumentasjon om dette i litteraturen men sunn fornuft tilsier at alle tiltak som reduserer ødemet bør være gunstig. Siden de fleste pasienter skal ha walkeren på dag og natt anbefaler vi en klasse 1 kompresjonsstrømpe, iallfall i starten for å teste at pasienter tåler kompresjonen. Etter hvert kan en eventuelt gå over til en klasse 2 strømpe. Husk at strømpen må sannsynligvis byttes ut allerede etter 2-4 uker, når hevelsen begynner å gå ned vil strømpen være for slakk og ikke passe ordentlig lenger.
Et generell råd er selvsagt også at pasienten skal holde foten elevert når han/hun hviler, dette vil også redusere ødemet raskere.
Medikamentell behandling i den akutte fasen:
Om pasienten har smerter bør pasienten tilbys analgetika etter vanlig smertebehandlings trinn. Her starter en som regel med Paracetamol 1 g x 3-4. Om ikke det er tilstrekkelig kan en legge til Kodein for eksempel 25 mg x 3, eller gå over til B- preparater som Paralginforte/Pinexforte som også inneholder Kodein. En bør unngå bruk av B- preparater i lengere enn 2 uker for å forhindre avhengighets symptomer. Tramadol kan være et alternativ for yngre pasienter (pasienter over 70 år tåler dette ofte dårligere). NSAIDS kan være aktuelt dersom pasienten ikke har kjent hjerte- eller nyre sykdom men vi har ikke funnet noe dokumentasjon i litteraturen om NSAIDS sin rolle ved behandling av Charcot fot. Det er sjelden behov for sterke smertestillende siden de fleste pasienter har nevropati med nedsatt følelsessans.
Husk at bakteriell infeksjon og Charcot fot kan forekomme samtidig. Om en ikke kan utelukke en infeksjon bør en, spesielt hos diabetikere, ha lav terskel til å starte opp med antibiotika. Om en mistenker at det kan foreligge en osteomyelitt (er nesten utelukket dersom pasienten ikke har sår) bør en sikre seg en benbiopsi før en starter opp for å vite hvilken bakterie en behandler. I noen tilfeller har en ikke tid til å vente på en slik biopsi, da kan en starte med antibiotika for å roe ned det verste av infeksjon og etter cirka 10-14 dager kan en seponere antibiotika. Etter ytterlige 2 uker etter at antibiotika er seponert kan en så ta en benbiopsi. Igjen, det beste er å ta en benbiopsi før antibiotika oppstart. Det er viktig å ikke starte opp med antibiotika bare for å være på den sikre siden, Charcot fot i seg selv (uten stor mistanke om samtidig infeksjon) skal ikke behandles med antibiotika.
Når det gjelder behandling av selve Charcot tilstanden finnes det ingen medikamenter som kan reversere tilstanden. Noen studier tyder på at bisfosfonater (for eksempel Fosamax) kan forsøkes for raskere å få en normalisering av forandringene i skjelettet. Her bruker en samme dosering som ved osteoporse generelt, en tablett ukentlig samt calcium tilskudd daglig. Dette er omstridt og i NICE guidelines er det kun svake anbefalinger for bruk av bisfosfonater. Vi bruker ofte bisfosfonater i behandlingen av denne tilstanden, og støtter oss på de få studiene som anbefaler denne praksisen. Det er vår erfaring at pasientene tåler denne behandlingen godt og det er forbundet med liten risiko. Husk at store deler av den eldre befolkningen i Norge bruker osteoporose medisin. Tatt i betraktning hvor alvorlige konsekvenser Charcot fot har, vil vi argumentere for at dersom studiene bare antyder en viss effekt er det verdt å prøve det. Det finnes noen få studier som konkluderer med at bisfosfonater kanskje har en negativ innvirkning på helingsprosessen i Charcot fot, så det er ingen fasit her.
Samme argumentene gjelder også for kalsitonin, et hormon som regulerer skjelettmetabolismen. Her finnes det noen studier som viser til en viss effekt. Igjen, er det for få studier til å tillate noen endelig konklusjon. Dersom en imidlertid har en pasient som ikke responderer ordentlig på behandling til tross for optimal avlastning og god compliance og hvor en har utelukket andre diagnoser med sikkerhet, bør en vurdere behandling med kalsitonin. Om en har en pasient som gjerne har prøvd bisfosfonatbehandling uten effekt, kan en vurdere daglige subkutane injeksjoner med 100 IE kalsitonin ( Miacalcic) i cirka 14-21 dager. For å få denne behandlingen dekket av HELFO må en sende inn særskilt søknad og oftest krever HELFO da at en har prøvd andre alternativer (for eksempel bisfosfonater) først. Igjen -merk at våre anbefalinger om bruk av bisfosfonater og kalsitonin er omstridt, og at det ikke finnes gode nok studier som kan konkludere med at en skal starte med slik behandling.
Charcot fot er en inflammatorisk sykdom og en skulle da tenke at inflammasjonsdempende midler som kortikosteroider kunne være gunstig. Ifølge de fleste artiklene tilgjengelig er kortikosteroider derimot kontraindisert. En mistenker at de kan forverre tilstanden, siden pasienter med diabetes som tar kortikosteroider er i økt risikogruppe for å utvikle Charcot fot.
Om pasienten er så hoven at også leggen er affisert må en som nevnt tidligere sjekke for dyp vene trombose (DVT). Om en ultralyd og blodprøvene avkrefter mistanken om DVT bør pasienten likevel settes på profylaktisk behandling med lavmolekulært heparin (Fragmin/ Klexane) siden hevelsen og samtidig bruk av en walker og immobilisering utgjør en additiv risiko for å utvikle blodpropp. Varigheten av behandling med Framin/Klexane er avhengig av varigheten av hevelsen men oftest bør det vare i minst 2 uker.
Post-akutt fasen
Når hevelsen er nesten borte og temperatur forskjellen holder seg konstant under 2 C° i forskjell over flere dager tyder det på at det akutte forløpet går over i det en kaller post-akutt fasen. Vi anbefaler at en fortsetter med en walker ortose til hevelsen er helt borte og foten igjen er normal temperert. Dette tar som nevnt tidligere oftest 3-6 mnd.
Når en klarerer pasienten for å kunne seponere bruken av walkeren trenger pasienten stort sett alltid spesial fotsenger og spesialsko, husk at det kan ta en måned før disse er ferdig laget hos ortopediingeniør, så bestill disse i tide slik at de ligger klar til bruk når ortosen seponeres!
Når pasienten starter med spesialskoene kan det hende at han/hun hovner opp igjen og at rødme og temperaturøkning kommer tilbake, da betyr det at en har seponert walkeren for tidlig og pasienten må belage seg på minst 4 nye uker med walkeren før en igjen forsøker med spesialsko.
Hvor lang tid tar det før en Charcot fot er helt utbrent? Noen studier antyder at det kan ta 1-2 år før alle inflammatoriske forandringer er helt borte. I denne tiden kan tilstanden blusse opp igjen dersom pasienter overbelaster eller får nye traume eller sår. Dette tilsier at pasienten må følges opp med hyppige kontroller på en sårpoliklinikk, for eksempel hver måned og pasienten må få kunne kontakte sårpoliklinikken ved minste antydning til forandringer. Det vil være fornuftig at pasienten kjøper seg et IR termometer som vist ovenfor for å selv kunne følge med eventuell forverring som stort sett alltid vil vise seg som en temperaturøkning i foten.
Om diagnosen var stilt for sent kan en dessverre ikke alltid forhindre at det tilkommer varige feilstillinger i foten. Om disse feilstillingene er så uttalte at de kan gi truende trykksår og om pasienten er relativ ung og har god sirkulasjon kan en vurdere operativ behandling med korreksjon av feilstillingene. Dette må aldri utføres før tilstanden er helt utbrent, altså ikke før det er gått cirka 2 år ellers kan en risikere at det blusser opp igjen da en operasjon representerer et nytt traume mot foten.
Operativ korreksjon av slike deformiteter er ofte veldig krevende kirurgi som bør kun utføres av en fotkirurg med spesialkompetanse i Charcot fot problematikk. Det er få ortopeder i Norge som er eksperter på dette området og om du har en pasient hvor du mener at korrigerende kirurgi kan være aktuelt vil vi anbefale at en henvender seg til ortopedisk avdeling på Ullevål Sykehus/OUS. Siden dette er et absolutt nisjeområde fordyper vi oss ikke i de forskjellige operasjonsteknikkene her.
Prognosen
For å få en optimal prognose bør tilstanden fanges opp så snart som mulig. Flere studier tyder på at prognosen forverres dersom det går mer enn 2 uker fra debut. Med korrekt behandling (altså total avlastning) tar det som regel 3-6 måneder før tilstanden «brenner ut». Om Charcot fot kun rammer forfoten er prognosen noe bedre og her brenner tilstanden oftest ut innen cirka 2-3 måneder under optimale forhold.
Dessverre blir diagnosen ofte stilt sent, oftest mange måneder for sent. Vi vil helst fange opp tilstanden før det kan sees forandringer i knoklene ved radiologiske undersøkelser. Når det allerede er tilkommet skjelettforandringer blir behandlingstiden vesentlig forlenget og i disse tilfellene kan det være behov for avlastning i et halvt år eller enda lenger.
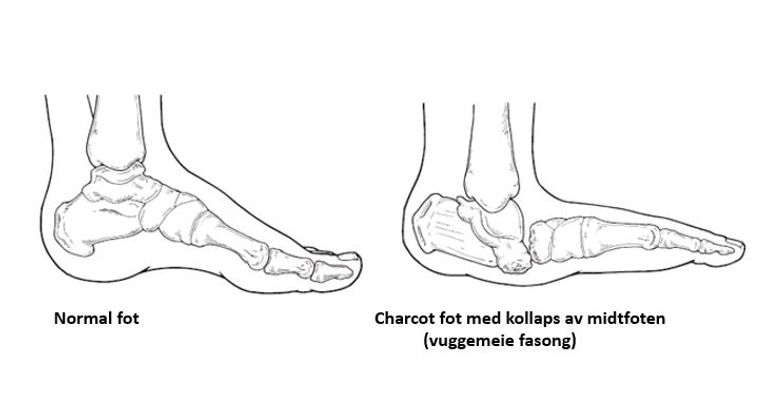
Figur 9 Dessverre stilles ofte diagnosen «Charcot fot» for sent og pasienten kan allerede ha utviklet deformiteter når diagnosen endelig fanges opp. Slike feilstillinger er permanente og gir en betydelig økt risiko for utvikling av fotsår.

Figur 10 En typisk vuggemeie fasong etter en for sent behandlet Charcot fot. Her er midtfoten kollapset og det er stor fare for utvikling av sår ved den største prominensen (rød pil)

Figur 11 Et typisk plantar sår hos en pasient med utbrent Charcot fot med vuggemeie deformitet. Bilde B viser et røntgenbilde hvor pilen viser den benete prominensen som trykker mot huden fra innsiden og skaper såret. Copyright: foot and ankle clinic, Victoria, Australia
Deformitetene som noen pasienter utvikler dersom tilstanden ikke fanges opp i tide fører nesten alltid til nye sår. Noen studier viser at pasientene som har gjennomgått Charcot artropati har en 30 ganger økt risiko for å utvikle et fotsår og cirka 60% av disse pasientene vil i senere forløpet utvikle et fotsår. Disse sårene er oftest nesten umulig å få til å gro fordi benstrukturene trykker på såret fra innsiden. Ikke sjelden fører dette til amputasjoner. Risikoen for en amputasjon hos en pasient med fotsår etter Charcot fot er cirka 12 x økt i forhold til andre pasienter med diabetes fotsår.
Konklusjon
Prognosen kan være meget god bare tilstanden fanges opp i tide. I motsatt tilfelle, altså når en ikke erkjenner tilstanden kan dette ha meget alvorlige konsekvenser for pasienten.
Referanser
Pakarinen TK, Laine HJ, Honkonen SE, Peltonen J, Oksala H, Lahtela J. Charcot arthropathy of the diabetic foot. Current concepts and review of 36 cases. Scand J Surg. 2002; 91(2):195-201.
Sanders LJ. What lessons can history teach us about the Charcot foot? Clin Podiatr Med Surg. 2008; 25(1):1-15.
Rogers LC, Bevilacqua NJ. Imaging of the Charcot foot. Clin Podiatr Med Surg. Apr 2008; 25(2):263-274.
Morrison WB, Schweitzer ME, Batte WG, Radack DP, Russel KM. Osteomyelitis of the foot: relative importance of primary and secondary MR imaging signs. Radiology. Jun 1998; 207(3):625-632.
Alnafisi N, Yun M, Alavi A. F-18 FDG positron emission tomography to differentiate diabetic osteoarthropathy from septic arthritis. Clin Nucl Med. Jul 2001; 26(7):638-639.
Rogers LC, Bevilacqua NJ. The diagnosis of Charcot foot. Clin Podiatr Med Surg. Jan 2008; 25(1):43-51.
Sanders LJ, Frykberg RG. The Charcot foot. In Frykberg (ed.): The high risk foot in diabetes mellitus. Churchill Livingstone, New York, 1991, pp. 325-335.
Armstrong DG, Todd WF, Lavery LA, Harkless LB. The natural history of acute Charcot’s arthropathy in a diabetic foot specialty clinic. Diabetic Medicine. 1997; 14(5):357-363.
Jude EB, Page S, Donohoe M, et al. Pamidronate in diabetic Charcot arthropathy: a randomised placebo controlled trial. Diabetologia. 2010:
Jude EB, Selby PL, Burgess J, et al. Bisphosphonates in the treatment of Charcot neuroarthropathy: a double-blind randomised controlled trial. Diabetologia. Nov 2001; 44(11):2032-2037.
Pitocco D, Ruotolo V, Caputo S, et al. Six-month treatment with alendronate in acute Charcot neuroarthropathy: a randomized controlled trial. Diabetes Care. May 1, 2005 2005; 28(5):1214-1215.
Bem R, Jirkovska A, Fejfarova V, Skibova J, Jude EB. Intranasal calcitonin in the treatment of acute Charcot neuroosteoarthropathy: a randomized controlled trial. Diabetes Care. Jun 2006; 29(6):1392-1394.
Armstrong DG, Sangalang MB, Jolley D, et al. Cooling the foot to prevent diabetic foot wounds: a proof-of-concept trial. J Am Podiatr Med Assoc. 2005; 95(2):103-107.
NIDDK NIH Summary Report Charcot Workshop, co-sponsored by NIH’s Office of Rare Diseases (2008), http://archives.niddk.nih.gov/ neuroarthropathy/SummaryReport.pdf,/neuroarthropathy/summaryreport.pdf
Sohn M-W, Lee Todd A, Stuck R, Frykberg R, Budiman-Mak E. Mortality risk of Charcot arthropathy compared with that of diabaetic foot ulcer and diabetes alone. Diabetes Care. 2009;32:816–21.
Rogers L, Frykberg R, Armstrong D, Boulton A, Edmonds M, Georges H, et al. The Charcot Foot in Diabetes. Diabetes Care. 2011;34(9):2123– 9
Wukich D, Sung W, Wipf AM, Armstrong D. The consequences of complacency: managing the effects of unrecognized Charcot feet. Diabet Med. 2011;28:195–8
Eichenholtz SN. Charcot Joints. IL, USA: Springfield; 1966.
Wukich D, Sung W. Charcot arthropathy of the foot and ankle: modern concepts and management review. J Diabetes Complications. 2009;23(6): 409–26.
Sommer TC, Lee TH. Charcot foot: the diagnostic dilemma. Am Family Physcian. 2001;64:1591–8.
Armstrong DG, Lavery LA, Liswood PJ, Todd WF, Tredwell JA. Infrared dermal thermometry for the high-risk diabetic foot. Phys Ther. 1997;77(2):169– 75. discussion 176–7
Petrova NL, Edmonds ME. Charcot neuro-osteoarthropathy-current standards. Diabetes Metab Res Rev. 2008;24 Suppl 1:S58–61.
Armstrong DG, Lavery LA. Monitoring healing of acute Charcot’s arthropathy with infrared dermal thermometry. J Rehabil Res Dev. 1997;34:317–21.
Najafi B, Wrobel JS, Grewal G, Menzies RA, Talal TK, Zirie M, et al. Plantar Temperature Response to Walking in Diabetes with and without Acute Charcot: The Charcot Activity Response Test. J Aging Res. 2012;2012:140968.
Stuck RM, Sohn MW, Budiman-Mak E, Lee TA, Weiss KB. Charcot Arthropathy Risk Elevation in the Obese Diabetic Population. Am J Med. 2008;121(11):1008–14.
Palestro CJ, Love C, Tronco GG, Tomas JN, Rini JN. Combined Labeled Leukocyte and Technetium 99 m Sulfur Colloid Bone Marrow Imaging for Diagnosing Musculoskeletal Infection 1. RadioGraphics. 2006;26:859–70.
Van Nostrand D, Abreu SH, Callaghan JJ, Atkins FB, Stoops HC, Savory CG. In-111–labeled white blood cell uptake in noninfected closed fracture in humans: prospective study. Radiology. 1988;167:495–8.
Palestro CJ, Torres MA. Radionuclide imaging in orthopedic infections. Semin Nucl Med. 1997;27:334–45.
Milne T, Rogers JR, Kinnear EM, Martin HV, Lazzarini PA, Quinton TR, et al. Developing an evidence-based clinical pathway for the assessment, diagnosis and management of acute Charcot Neuro-Arthropathy: a systematic review. J Foot Ankle Res. 2013;6:30
Pakarinen TK, Laine J, Honkonen E, Peltonen J, Oksala H, Lahtela J. Charcot Arthropathy of the Diabetic Foot. Current Concepts and Review of 36 Cases. Scand J Surg. 2002;91(2):195–201
Munichoodappa C, Kozak G. Neuroarthropathy (Charcot Joints) In Diabetes Mellitus. Medicine. 1972;51(3):191–210
Fabrin J, Larsen K, Holstein PE. Long term follow up in diabetic Charcot feet with spontaneous onset. Diabetes Care. 2000;23(6):6796–800
Koeck FX, Bobrik V, Fassold A, Grifka J, Kessler S, Straub R. Marked loss of sympathetic nerve fibers in chronic Charcot foot of diabetic origin compared to ankle joint osteoarthritis. J Orthop Res. 2009;27(6):736–41
Frykberg R, Belczyk R. Epidemiology of the Charcot Foot. Clin Podiatr Med Surg. 2008;25(1):17–28
Petrova NL, Foster VM, Edmonds ME. Calcaneal bone mineral density in patients with Charcot neuropathic osteoarthropathy: differences between Type 1 and Type 2 diabetes. Diabet Med. 2005;22:756–61
Sohn MW, Stuck R, Pinzur M, Lee T, Budiman-Mak E. Lower-Extremity Amputation Risk after Charcot Arthropathy and Diabetic Foot Ulcer. Diabetes Care. 2010;33:98–100.
Rogers L, Bevilacqua N. Imaging of the Charcot Foot. Clin Podiatr Med Surg. 2008;25:43–51
Rogers L, Frykberg R. The Charcot Foot. Med Clin N Am. 2013;97:847–56.
Sanders LJ, Mrdjenovich D. Anatomical patterns of bone and joint destruction in neuropathic diabetics. Diabetes. 1991;40 Suppl 1:529A
Sanders LJ, Frykberg RG. Diabetic Neuropathic Osteoarthropathy: The Charcot Foot, 297–338. In: Frykberg RG, editor. The High Risk Foot In Diabetes Mellitus. New York: Churchill Livingstone; 1991.
Armstrong D, Lavery L. The natural history of acute Charcot’s arthropathy in a diabetic foot specialty clinic. Diabet Med. 1997;14:357–63.



















